Chronisch obstruktive Lungenerkrankung (COPD) – Medikamentöse Therapie
Therapieziele
- Nikotinrestriktion (Verzicht auf Tabakkonsum inkl. Passivrauchen) [einziger kausaler Therapieansatz!]
- Symptomlinderung
- Verbesserung der Belastbarkeit
- Verhinderung von Krankheitsprogression (Fortschreiten der Krankheit) und Exazerbationen (deutliche Verschlimmerung der Symptome)
Therapieempfehlungen
Bei der chronisch obstruktiven Lungenerkrankung (COPD) wird je nach Schweregrad nach folgenden Stufenschema vorgegangen:
| Inhalative Bronchodilatatoren (Arzneimittel, welche die Bronchien erweitern) bei Bedarf |
Inhalative Bronchodilatatoren als Dauertherapie |
Inhalative Glucocorticoide (Synonym: inhalative Steroide, ICS) |
Sauerstofftherapie bis zu 16-24 h/d |
|
| Grad 1 (leicht) |
+ |
- |
- |
- |
| Grad 2 (mittelschwer) |
+ |
+ |
- |
- |
| Grad 3 (schwer) |
+ |
+ |
+ |
- |
| Grad 4 (sehr schwer) |
+ |
+ |
+ |
+ |
Mit keinem der dargestellten Medikamente kann das Fortschreiten der Erkrankung verhindert werden.
Beachte: FLAME-Studie: LAMA/LABA-Kombination (Indacaterol und Glycopyrronium) schützt bei schwerer COPD besser vor Exazerbationen als die Kombination ICS/LABA (Indacaterol und Glycopyrronium) [11].
Behandlung der stabilen COPD gemäß der „Global Initiative for Chronic Obstructive Lung Disease (GOLD)“ (2019) [modifiziert nach Leitlinie: 3].
Initiale pharmakologische Behandlung
| Gruppe | Wirkstoffe | |
| 0 oder 1 moderate Exazerbation (ohne Hospitalisierung | A |
Bronchodilator
|
| B |
|
|
| ≥ 2 moderate Exazerbationen oder ≥ 1 mit Hospitalisierung | C |
|
|
||
| D |
|
|
|
Legende
- LABA: long-acting beta-2-agonists (Beta-2-Sympathomimetika)
- LAMA: Long Acting Muscarinic Antagonist (lang-wirksame Muskarin-Antagonisten; bronchienerweiternde Wirkstoffe aus der Gruppe der Parasympatholytika)
- ICS (Inhaled Corticosteroids): inhalative Steroide
Follow-up pharmakolgische Behandlung
- Wenn das Ansprechen auf die Erstbehandlung gut ist, behalten Sie sie bei.
- Falls nicht:
- Betrachten Sie das vorherrschende zu behandelnde Merkmal (Dyspnoe oder Exazerbationen) Verwenden Sie den Exazerbationsweg, wenn wohl Exazerbationen als auch Dyspnoe angegangen werden müssen.
- Starten Sie von dem Feld, das der aktuellen Behandlung des Patienten entspricht und folgen Sie den Anweisungen • Antwort bewerten, anpassen und überprüfen.
- Diese Empfehlungen hängen nicht von der ABCD-Beurteilung zum Zeitpunkt der Diagnose.
Dyspnoe (Atemnot)
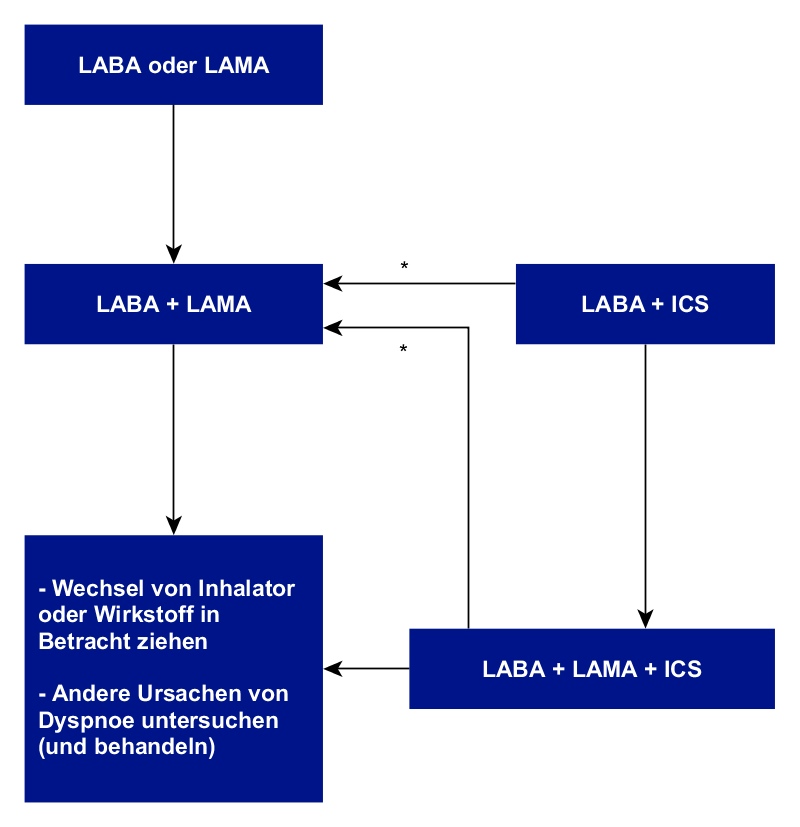
*Deeskalation von ICS oder Wechsel in Betracht ziehen bei: Pneumonie, nicht zutreffende ursprüngliche Indikation oder fehlendem Ansprechen auf ICS
Exazerbation (Verschlimmerung, zeitweise Steigerung, Wiederaufleben einer Krankheit)
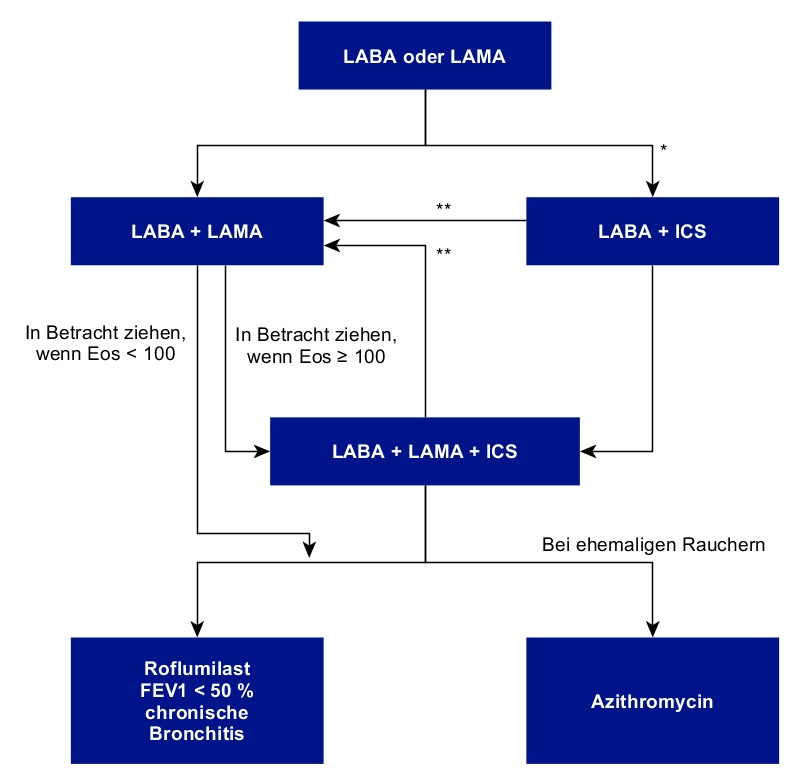
Legende
- Eos = Eosinophile Granulozyten (absolute Zahl/µl)
- *In Betracht ziehen, wenn Eos ≥ 300 oder ≥ 100 UND ≥ 2 moderate Exazerbationen/1 Hospitalisierung
- ** Deeskalation von ICS oder Wechsel in Betracht ziehen bei: Pneumonie, nicht zutreffende ursprüngliche Indikation oder fehlendem Ansprechen auf ICS
Beachte
- Eosinophile im Blut (≥ 300/µl Blut) und die Exazerbationsrate entscheiden bei COPD, ob ein inhalierbares Corticosteroid (ICS) eingenommen werden soll oder nicht (aktueller Standard); Ergebnisse mit Benralizumab (anti-eosinophiler, humanisierter, afucosylierter, monoklonaler Antikörper (IgG1, kappa) waren viel besser als mit Cortison: um eine Exazerbation innerhalb von 90 Tagen zu verhindern, mussten nur vier Patienten den Antikörper anstelle von Cortison erhalten (Number Needed to Treat = 4) [17].
Weitere Hinweise
- Grundlage der Therapie sind langwirksame Anticholinergika (LAMA) und Beta-2-Sympathomimetika (LABA).
- Maximale Bronchodilatation (Erweiterung der Bronchien) ist nur mittels Kombination von LAMA (Long Acting Muscarinic Antagonist)) und LABA (long-acting beta-2-agonists) möglich.
FLAME-Studie: LAMA/LABA-Kombination schützt bei schwerer COPD besser vor Exazerbationen als die Kombination ICS/LABA [11]. - Patienten, die unter einem Beta-2-Mimetikum über Palpitationen (Herzstolpern) klagen, sind mit einem Anticholinergikum besser bedient.
- Inhalative Glucocorticoide (Synonym: inhalative Steroide, ICS):
- Die Dosis-Wirkungskurve der Steroide ist sehr flach, d. h. eine Hochdosistherapie ist im Regelfall nicht erforderlich!
- In einer Studie konnte gezeigt werden, dass LABA plus LAMA bei Patienten mit einer schweren chronisch obstruktiven Lungenerkrankung, die Therapie mit inhalativen Steroiden beendet werden konnte, ohne dass es zu einer Zunahme der Exazerbationen kam. Es kam jedoch auch zu einem stärkeren Abfall des FEV1 (43 mL) als bei weiterer Steroidtherapie. In beiden Gruppen ergab sich kein Unterschied für die Dyspnoe (Atemnot) [3].
- Weitere Fakten zu ICS [10]:
- bei COPD deutlich schwächer wirksam als bei Asthma bronchiale
- ICS senkt die COPD-Exazerbationsrate (Verschlechterung des Krankheitsbildes); die Effektivität ist mit steigendem Anteil Eosinophiler im Blut erhöht
- gemäß erster Tabelle werden ICS nachrangig Bronchodilatatoren eingesetzt
- ICS-Effekt auf die Reduktion des jährlichen FEV1-Verlusts ist klinisch nicht bedeutungsvoll
- ICS können bei stabilen COPD Patienten schrittweise reduziert werden
- Indikation für den Einsatz von ICS ist regelmäßig zu überprüfen. Absetzen, wenn die Zahl der Eosinophilen im Differentialblutbild < 100 Zellen/μl beträgt und keine klinischen asthmatischen Komponenten vorhanden sind.
- Beachte: Inhalative Corticosteroide (ICS) erhöhen bei COPD-Patienten das Risiko für eine Infektion mit nichttuberkulösen Mykobakterien [13].
- Betablocker:
- COPD-Patienten mit Gold-Stadium 3 und 4 profitieren von den bronchokonstriktiven Effekten der Betablocker (Betablockade), d. h. dass bei Einnahme von Betablockern die Exazerbationen zurückgingen [6].
- Eine Betablocker-Therapie bei Patienten mit kardialer Erkrankungen und COPD senkte das Mortalitätsrisiko (Sterberisiko). Bei Patienten mit einem kardioselektiven Betablocker (Metoprolol, Bisoprolol, Atenolol, Nebivolol) war das Risiko für eine Exazerbation sogar um 28 Prozent reduziert. Die Mortalität (Sterberate) wurde durch Betablockade um 30 % reduziert (im Vergleich zu Patienten ohne Betablocker). Die Risikoreduktion betrug für kardioselektive Wirkstoffe 40 % und nichtselektive Wirkstoffe 26 % [14].
- Inhalative Glucocorticoide (Synonym: inhalative Steroide, ICS) erhöhen das Risiko
- einer schweren Pneumonie (Lungenentzündung): Fluticason erhöhte die Zahl der schweren Pneumonien (die einen Krankenhausaufenthalt erforderlich machten) um 78 % (Odds-Ratio,78, 95-Prozent-Konfidenzintervall: 1,50-2,12) [8].
- einer Pseudomonas-aeruginosa-Besiedelung; das Risiko steigt mit der ICS-Dosis [15]
- Die Fixkombination zweier Bronchodilatatoren (LAMA + LABA) wird Kombination der ersten Wahl für alle COPD-Patienten werden; auch bzgl des primären Endpunkts "jährliche Exazerbationsrate" war diese Fixkombination dem bisherigen Therapiestandard überlegen [9].
- Inhalierbares Corticosteroid (ICS): Eosinophile im Blut (= Prädiktor für das Ansprechen auf ICS) und die Exazerbationsrate entscheiden bei COPD, ob ein inhalierbares Corticosteroid (ICS) eingenommen werden soll oder nicht.
Bei Patienten mit einer Eosinophilenzahl von über 300/μl sollte das ICS nicht abgesetzt werden [Leitlinien: ERS] - LABA/LAMA/ICS-Dreifachtherapie versus LABA/LAMA‐Zweifachtherapie: Evidenz von hoher Vertrauenswürdigkeit zeigt, dass sich die Lebensqualität der Betroffenen mit der Dreifachtherapie im Vergleich zur LABA/LAMA‐Zweifachtherapie verbessert [16].
- Dupilumab: Indikation: Add-on-Erhaltungstherapie für Erwachsene mit unkontrollierter COPD und Zeichen einer Typ-2-Inflammation (Eosinophilenzahl im Blut von ≥ 300 Zellen/μl).
Nebenbedingung: Patienten, die bereits eine Kombination aus einem inhalativen Kortikosteroid (ICS), einem langwirksamen Beta-2-Agonisten (LABA) und einem langwirksamen Muskarinantagonisten (LAMA) oder eine Kombination aus einem LABA und einem LAMA erhalten, wenn ein ICS nicht angebracht ist. -
Siehe am Ende dieses Artikels auch Informationen zu den typischen Komorbiditäten der COPD.
Sauerstoffgabe bei schweren Exazerbationen der COPD
- Sauerstoffgabe zur adäquaten Oxygenierung und Entlastung der Atemmuskulatur.
Beachte: Die nicht invasive Sauerstoffgabe (noninvasive ventilation, NIV) war verglichen mit der invasiven Sauerstoffgabe (invasive mechanical ventilation, IMV) mit einer geringeren Mortalität (Sterberate), geringerem Risiko für nosokomiale Pneumonien (Lungenentzündungen als Krankenhausinfektion) und kürzeren Klinikaufenthalt assoziiert [5].
Kardiovaskuläre Erkrankungen und COPD
Hypertonie (Bluthochdruck), Koronare Herzkrankheit (KHK, Herzkranzgefäßerkrankung), Herzinsuffizienz (Herzschwäche) und Vorhofflimmern (VHF) sind die häufigsten Komorbiditäten (Begleiterkrankungen) der COPD. Dieses kann bei COPD-Patienten mit KHK und Herzinsuffizienz den Einsatz gegensätzlicher Therapieprinzipien erforderlich machen. Die GOLD-Leitlinie empfiehlt in diesen Fällen so zu behandeln, als hätten diese keine COPD. Dabei sollten allerdings kardioselektive ("herzwirksame") Wirkstoffe wie Bisoprolol den Vorzug gegeben werden [4]. Siehe dazu auch nachfolgend unter dem Titel “Postmyokard-Therapie bei CPO bei COPD“.
Postmyokardinfarkt-Therapie bei COPD
Die Zurückhaltung mit Betablockern bei COPD-Patienten mit akutem Myokardinfarkt (Herzinfarkt) sollte aufgegeben werden: Das Mortalitätsrisiko der Patienten mit neu begonnener Betablockade ist laut einer Studie während der knapp dreijährigen Nachbeobachtungszeit um 50 % geringer als das der Patienten ohne Betablocker [2].
Supplemente (Nahrungsergänzungsmittel; Vitalstoffe)
Geeignete Nahrungsergänzungsmittel sollten die folgenden Vitalstoffe enthalten:
- Vitamine (A, C, E, D3, K, B1, B2, Niacin (Vitamin B3), Pantothensäure (Vitamin B5), B6, B12, Folsäure, Biotin)
- Mineralstoffe (Calcium, Chlorid, Kalium, Magnesium, Natrium, Phosphor)
- Spurenelemente (Chrom, Eisen, Fluorid, Jod, Kupfer, Mangan, Molybdän, Selen, Zink)
- Fettsäuren (Omega-3-Fettsäuren: Alpha-Linolensäure (ALA), Eicosapentaensäure (EPA) und Docosahexaensäure (DHA); Omega-6-Fettsäuren: Linolsäure)
- Weitere Vitalstoffe (Fruchtsäuren – Citrat (gebunden in Magnesium-, Kalium- und Calciumcitrat))
Bei Vorliegen einer Insomnie (Schlafstörung) infolge einer chronisch obstruktiven Lungenerkrankung s. u. Insomnie/Medikamentöse Therapie/Supplemente.
Beachte: Die aufgeführten Vitalstoffe sind kein Ersatz für eine medikamentöse Therapie. Nahrungsergänzungsmittel sind dazu bestimmt, die allgemeine Ernährung in der jeweiligen Lebenssituation zu ergänzen.
Für Fragen zum Thema Nahrungsergänzungsmittel stehen wir Ihnen gerne kostenfrei zur Verfügung.
Nehmen Sie bei Fragen dazu bitte per E-Mail – info@docmedicus.de – Kontakt mit uns auf, und teilen Sie uns dabei Ihre Telefonnummer mit und wann wir Sie am besten erreichen können.
Literatur
- Leppi JD et al.: Short-term vs conventional glucocorticoid therapy in acute exacerbations of chronic obstructive pulmonary disease. JAMA 2013; 309: 2223-31
- Quint JK et al.: Effect of β blockers on mortality after myocardial infarction in adults with COPD. BMJ 2013;347:f6650; doi: 10.1136/bmj.f6650
- Magnussen H et al.: Withdrawal of Inhaled Glucocorticoids and Exacerbations of COPD. N Engl J Med 2014; 371:1285-1294, October 2, 2014, doi: 10.1056/NEJMoa1407154
- Ni Y, Shi G, Wan H. Use of cardioselective beta-blockers in patients with chronic obstructive pulmonary disease: a meta-analysis of randomized, placebo-controlled, blinded trials. J Int Med Res. 2012;40:2051-2065
- Lindenauer K et al.: Outcomes associated with invasive and noninvasive ventilation among patients hospitalized with exacerbations of chronic obstructive pumonary disease. JAMA Intern Medd 2014;174: 192-93
- Bhatt SP et al.: β-Blockers are associated with a reduction in COPD exacerbations. Thorax doi:10.1136/thoraxjnl-2015-207251
- Aclidiniumbromid – Nutzenbewertung gemäß § 35a SGB V 12.01.2016; IQWiG
- Kew KM et al.: Inhaled steroids and risk of pneumonia for chronic obstructive pulmonary disease. doi: 10.1002/14651858.CD010115.pub2
- Wedzicha JA et al.: Indacaterol – Glycopyrronium versus Salmeterol–Fluticasone for COPD. May 15, 2016, doi: 10.1056/NEJMoa1516385
- Gillissen A, Haidl P, Kohlhäufl M, Kroegel K, Voshaar T, Gessner C: The pharmacological treatment of chronic obstructive pulmonary disease. Dtsch Arztebl Int 2016; 113: 311-6. doi: 10.3238/arztebl.2016.0311
- American Thoracic Society International Conference, San Francisco 13-18. Mai 2016; J.A. Wedzicha, et al.: Indacaterol-Glycopyrronium versus Salmeterol-Fluticasone for COPD. N Engl J Med 2016, doi: 10.1056/NEJMoa1516385
- Vogelmeier CF et al.: Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Lung Disease 2017 Report. GOLD Executive Summary. Am J Respir Crit Care Med. 2017 Mar 1;195(5):557-582. doi: 10.1164/rccm.201701-0218PP.
- Brode SK et al.: The risk of mycobacterial infections associated with inhaled corticosteroid use. European Respiratory Journal 2017 50: 1700037; doi: 10.1183/13993003.00037-2017
- Yang YL et al.: Association of β-blocker use with survival and pulmonary function in patients with chronic obstructive pulmonary and cardiovascular disease: a systematic review and meta-analysis. European Heart Journal 200;41 (46):4415-4422, https://doi.org/10.1093/eurheartj/ehaa793
- Eklöf J et al.: Use of inhaled corticosteroids and risk of acquiring Pseudomonas aeruginosa in patients with chronic obstructive pulmonary disease. Thorax 2021 doi:10.1136/ thoraxjnl-2021-217160
- van Geffen WH, Tan DJ, Walters JAE, Walters EH: Inhaled corticosteroids with combination inhaled long‐acting beta2‐agonists and long‐acting muscarinic antagonists for chronic obstructive pulmonary disease. Cochrane Database of Systematic Reviews 2023, Issue 12. Art. No.: CD011600. doi: 10.1002/14651858.CD011600.pub3
- Ramakrishnan S et al.: Treating eosinophilic exacerbations of asthma and COPD with benralizumab (ABRA): a double-blind, double-dummy, active placebo-controlled randomised trial Lancet Respiratory Medicine 2024
Leitlinien
- Global Initiative for Chronic Obstructive Lung Disease (GOLD): 2019 GOLD Report. Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. www.goldcopd.org
- Chalmers JD et al.: Withdrawal of inhaled corticosteroids in COPD: a European Respiratory Society guideline European Respiratory (ERS) Journal 2020 55: 2000351; doi: 10.1183/13993003.00351-2020
- S2k-Leitlinie: Fachärztliche Diagnostik und Therapie der COPD. (AWMF-Registernummer: 020 - 006), Februar 2026 Langfassung